2026年3月11日,我校生命科学学院张水军教授课题组在《Nature Communications》期刊在线发表了题为《The conserved human astrovirus-receptor interface reveals a targetable vulnerability for antiviral development》的研究论文。该研究首次解析了人星状病毒8型(HAstV8)刺突蛋白与FcRn受体的复合物晶体结构,揭示了经典人星状病毒识别受体的保守分子机制,更重要的是,研究发现三款临床已获批的FcRn阻断剂能够通过竞争受体结合有效抑制星状病毒感染,有望通过“老药新用”的策略用于星状病毒治疗。

人星状病毒(HAstV)是全球儿童和老年人病毒性肠炎的主要病原体之一,约占非细菌性肠胃炎病例的10%,位列轮状病毒、诺如病毒之后,是第三大急性腹泻病毒病原,目前尚无获批的疫苗和特异性抗病毒药物,临床治疗面临巨大挑战。尽管有研究已证实FcRn是经典人星状病毒的入侵受体,但病毒与受体的具体结合机制及靶向该相互作用的抗病毒策略尚未明确。
针对以上问题,研究团队成功解析了分辨率为2.65 Å的HAstV8刺突蛋白-FcRn复合物晶体结构,以及HAstV1和HAstV8刺突蛋白的单体晶体结构。结构分析表明,HAstV8刺突蛋白通过其表面由四条β链形成的保守凹陷区域,与FcRn的α2结构域结合。序列比对进一步证实,该结合区域在所有八种经典人星状病毒血清型中高度保守(图1),揭示了经典人星状病毒利用FcRn入侵的共同分子基础。
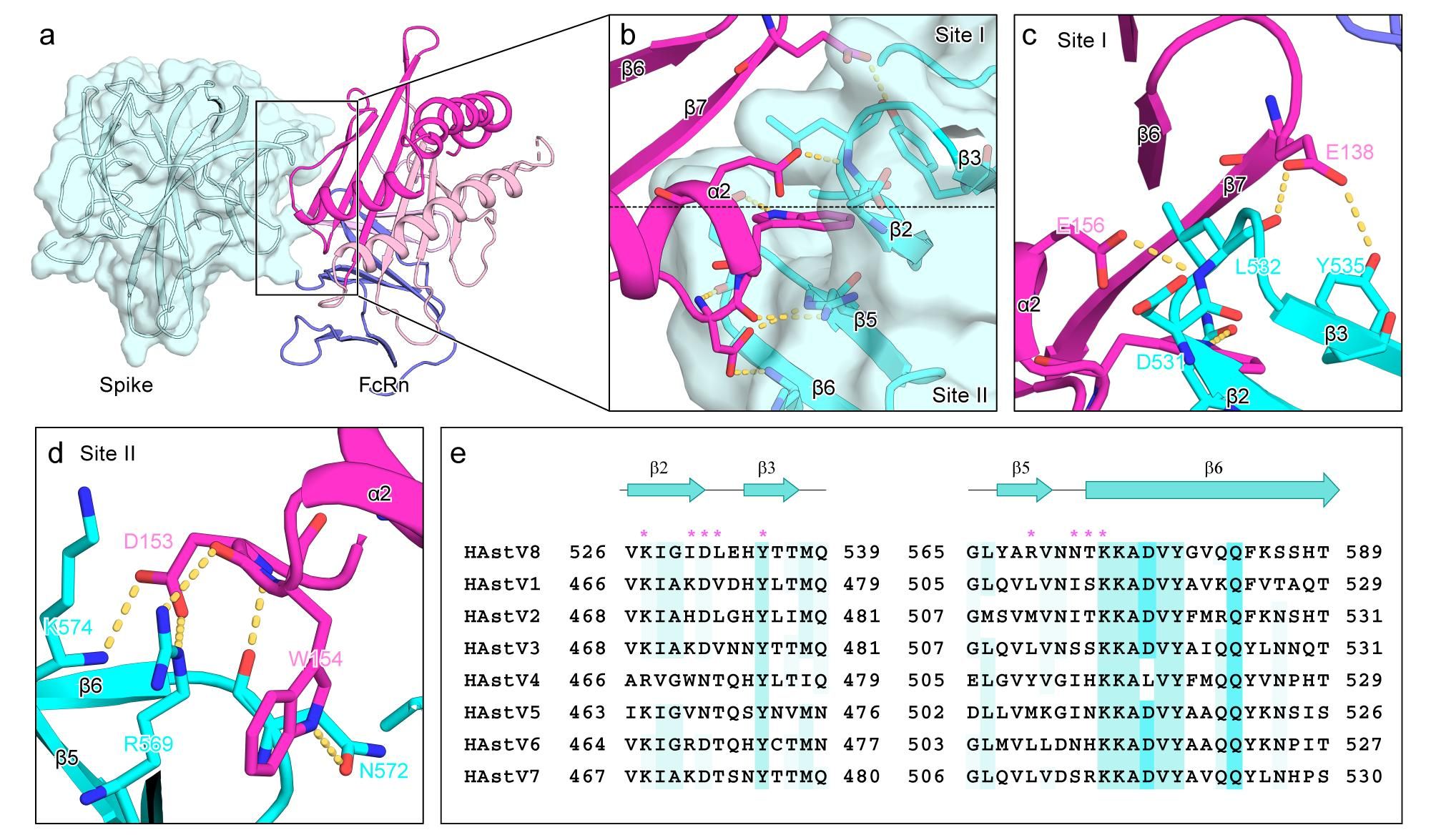
图1 HAstV8刺突蛋白通过由四条β链(β2、β3、β5和β6)形成的表面凹陷结构,与FcRn的α2结构域结合
值得注意的是,HAstV8刺突蛋白与三种临床获批用于治疗重症肌无力的FcRn阻断剂在FcRn上的结合位点高度重叠,为开发抗广谱病毒药物奠定了结构基础。基于这一结构发现,研究团队进一步评估了三种临床获批用于治疗重症肌无力的FcRn阻断剂—efgartigimod、rozanolixizumab和nipocalimab的抗病毒效果。实验结果表明,rozanolixizumab和nipocalimab能高效竞争性抑制星状病毒与FcRn的结合,显著阻断病毒对易感Caco2细胞的感染,使细胞内病毒RNA水平降低约90%;efgartigimod也表现出一定的抗病毒活性(图2)。这一发现证实了临床获批的FcRn阻断剂具有抑制星状病毒感染的潜力,为星状病毒感染的治疗提供了可直接进行临床转化的候选药物。
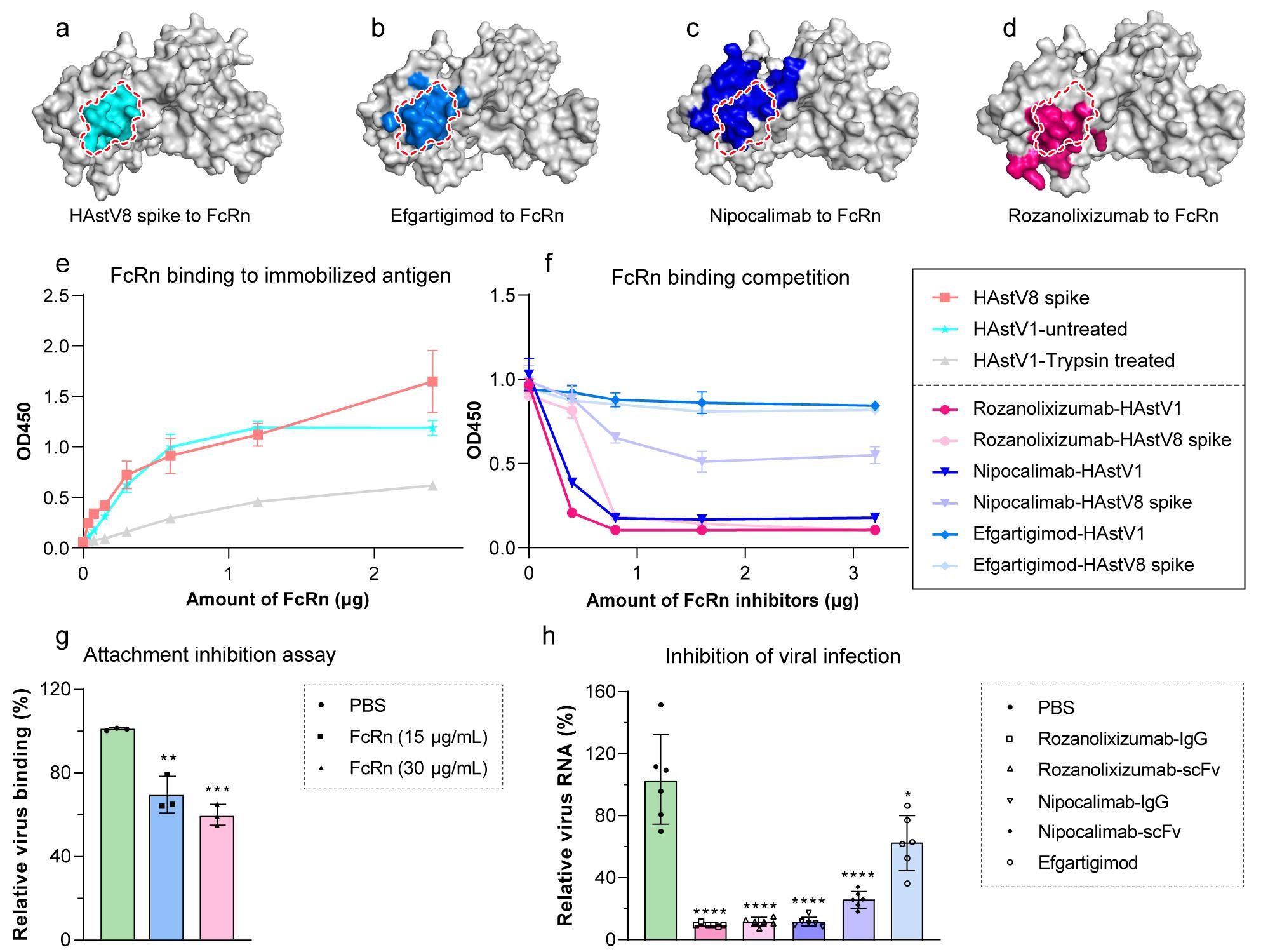
图2 可溶性FcRn及治疗性FcRn阻断剂抑制HAstV感染
该研究成果不仅揭示了人星状病毒利用FcRn受体的识别机制,填补了星状病毒入侵分子机制领域的研究空白,更为抗病毒药物的开发提供了全新的靶标,有望通过“老药新用”的策略用于星状病毒治疗,具有重要的理论意义和临床应用价值。
我校生命科学学院张水军教授、中国科学院武汉病毒所柯贤良助理研究员、中国疾病预防控制中心病毒病预防控制所孙晓曼副研究员、浙江大学医学院刘越教授为论文共同通讯作者,我校生科院博士研究生王炜、徐颖副教授为论文共同第一作者。该研究得到了国家自然科学基金、江苏省自然科学基金和中央高校基本业务费等项目的资助。
论文链接:
https://www.nature.com/articles/s41467-026-70465-5
编辑:徐颖
校对:李娜
审核:陈熙
